En los últimos años, la definición de fármaco exitoso ha cambiado. La época en la que un medicamento era un éxito de ventas ha finalizado, puesto que ya no tenemos enfermedades que puedan ser tratadas con un único fármaco. Y al mismo tiempo, los pacientes y mercados exigen medicinas más eficaces.
Pero esta demanda se hace cada vez más difícil de cumplir, ya que nuestro entendimiento de las enfermedades se hace más y más complejo, a lo que hay que añadir presiones externas (por parte de agencias reguladoras, de instituciones financieras, de los gobiernos e incluso de científicos) para alcanzar los mejores resultados clínicos.
Luego, ¿cómo es posible producir nuevos fármacos cuando sus costes de desarrollo se incrementan año tras año y es más complicado crearlos con un beneficio clínico para los pacientes?
Pero esta demanda se hace cada vez más difícil de cumplir, ya que nuestro entendimiento de las enfermedades se hace más y más complejo, a lo que hay que añadir presiones externas (por parte de agencias reguladoras, de instituciones financieras, de los gobiernos e incluso de científicos) para alcanzar los mejores resultados clínicos.
Luego, ¿cómo es posible producir nuevos fármacos cuando sus costes de desarrollo se incrementan año tras año y es más complicado crearlos con un beneficio clínico para los pacientes?
Para ello la ciencia nos ha proporcionado nuevas herramientas, como la capacidad de mapear el genoma humano (a un coste cada vez inferior) y de este modo, entender la expresión de diferentes proteínas en respuesta a diferentes enfermedades.
Como consecuencia, existe la idea de que la medicina personalizada, que utiliza este nuevo tipo de herramientas, pueda conducir hacia nuevas soluciones en el proceso de desarrollo de fármacos, medicamentos específicos que sean más eficaces e incluso más seguros.
Como consecuencia, existe la idea de que la medicina personalizada, que utiliza este nuevo tipo de herramientas, pueda conducir hacia nuevas soluciones en el proceso de desarrollo de fármacos, medicamentos específicos que sean más eficaces e incluso más seguros.
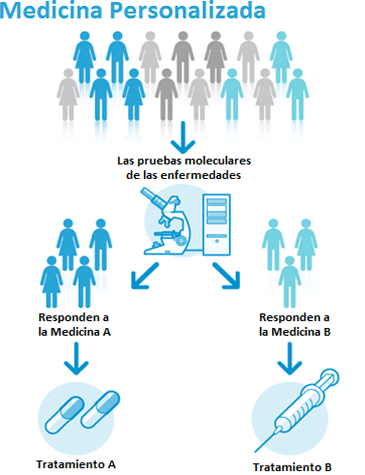
Pero, ¿cómo se define un medicamento personalizado?, por medicina personalizada se entiende aquel tratamiento médico diseñado a la medida de las características individuales de cada paciente. Se espera que, tanto en sus tratamientos preventivos como terapéuticos, actúen exclusivamente en aquellos pacientes que puedan beneficiarse realmente de estas terapias, evitando usarse en otros que no vean ningún tipo de beneficio en su administración.
Al actuar de esta manera, no sólo se mejora la capacidad para tratar enfermedades, sino también, potencialmente, implica un ahorro económico en el proceso.
Al actuar de esta manera, no sólo se mejora la capacidad para tratar enfermedades, sino también, potencialmente, implica un ahorro económico en el proceso.
En la medicina personalizada se distinguen tres categorías:
▣ Diagnóstico: productos que pueden diagnosticar el riesgo de padecer una enfermedad, la presencia real de una enfermedad en un individuo, o incluso guiar el tratamiento en personas que ya han sido diagnosticadas con una afección específica.
▣ Pruebas diagnósticas con fines terapéuticos: en esta categoría se trabaja codo con codo con un tratamiento farmacológico, indicando al médico acerca del tipo de medicamentos que un paciente en particular debería recibir.
▣ Herramientas de cribado: poseen la finalidad de detectar enfermedades en etapas tempranas, lo que permite una intervención rápida con la esperanza de reducir los efectos provocados por la enfermedad.
Idealmente, lo que interesaría es hallar la manera de evaluar el riesgo de una persona a una enfermedad o su respuesta a cierto tratamiento antes incluso de administrárselo.
Con la medicina personalizada seríamos capaces de conocer de antemano qué personas responderían a un fármaco específico y cuáles no, quienes presentarían graves efectos secundarios y cuáles no, quienes lo precisarían en una fase más temprana y quienes en una fase más tardía, todo ello con el objetivo de obtener los mejores resultados posibles en cada individuo.
Con la medicina personalizada seríamos capaces de conocer de antemano qué personas responderían a un fármaco específico y cuáles no, quienes presentarían graves efectos secundarios y cuáles no, quienes lo precisarían en una fase más temprana y quienes en una fase más tardía, todo ello con el objetivo de obtener los mejores resultados posibles en cada individuo.
La medicina personalizada ha experimentado un espectacular crecimiento en los últimos años pasando de 13 productos comercializados en el año 2006 a 72 en el año 2011.
En la actualidad, el 94% de las compañías biofarmacéuticas están investigando en medicina personalizada, ya que son conscientes de que su uso como herramienta de investigación o su utilización junto con un producto comercializado puede realmente mejorar el potencial que ese fármaco tenga en los pacientes.
Así mismo, sus ventas también se han visto incrementadas alcanzando una cifra anual de 30.000 millones de dólares de este tipo de productos en los USA.
En la actualidad, el 94% de las compañías biofarmacéuticas están investigando en medicina personalizada, ya que son conscientes de que su uso como herramienta de investigación o su utilización junto con un producto comercializado puede realmente mejorar el potencial que ese fármaco tenga en los pacientes.
Así mismo, sus ventas también se han visto incrementadas alcanzando una cifra anual de 30.000 millones de dólares de este tipo de productos en los USA.
Entre los productos pertenecientes a la medicina personalizada que son actualmente empleados por los médicos para tratar a sus pacientes destacan:
▣ La prueba BRACAnalysis que identifica mutaciones potenciales en los genes BRCA1 y BRCA2 responsables de la mayoría de cánceres hereditarios de mama y ovario. Dependiendo de la existencia o no de esas mutaciones se determina la probabilidad del paciente a desarrollar estos tipos de cáncer en el futuro, y en función de ello guiar también en la toma de decisiones a otros miembros familiares.
▣ Prueba Oncotype DX es una prueba de 21 genes que predice la probabilidad de beneficiarse de la quimioterapia y el riesgo de recurrencia del cáncer en los próximos 10 años.
▣ PreDX es un test sanguíneo que estudia los niveles de siete marcadores de progresión de la diabetes en sangre. Estos marcadores están relacionados con la calidad del tejido adiposo, el estado inflamatorio pancreático y el metabolismo de la glucosa.
Entre los beneficios actuales aportados por la medicina personalizada se encuentran:
▣ Una reducción del 34% en la quimioterapia aplicada a mujeres que padecen cáncer de mama y que previamente al tratamiento se han realizado un test genético.
▣ Hasta 17.000 derrames cerebrales podrían prevenirse anualmente en aquellos pacientes que son propensos a ello al administrarles la dosis apropiada de warfarina[1] siempre y cuando el correspondiente test genético se lleve a cabo.
▣ Un ahorro por encima de los 600 millones anuales en el sistema sanitario de los Estados Unidos si los pacientes que presentasen cáncer colorrectal con metástasis recibiesen el test del gen KRAS[2] anterior a su tratamiento.
▣ Desarrollo de nuevas herramientas de diagnóstico que pueden ayudar de diversas maneras en el proceso de desarrollo de fármacos. Así, si las compañías farmacéuticas conocen con anterioridad qué pacientes responderán mejor a un ensayo clínico, se obtendrán mejores resultados en dicho estudio.
Nos encontramos todavía en las primeras etapas de la medicina personalizada con un largo camino por recorrer durante los próximos años. La medicina personalizada nos ayudará a entender mejor las afecciones asociadas con distintas enfermedades, la identificación de nuevas dianas terapéuticas, la reducción de efectos secundarios y al incorporarla en nuestros experimentos y método de investigación se producirán innovaciones en el proceso de descubrimiento de nuevos medicamentos.
[1] Anticoagulante empleado en la prevención de trómbolos y émbolos.
[2] Gen que elabora la proteína KRAS que participa en las vías de señalización celular, en el crecimiento celular y la apoptosis.
[2] Gen que elabora la proteína KRAS que participa en las vías de señalización celular, en el crecimiento celular y la apoptosis.
Fuentes: UTAustinX: UT.4.01x Take Your Medicine - The Impact of Drug Development.
http://www.patia.com.mx/braca.html
https://breast-cancer.oncotypedx.com/es-MX/Professional-Invasive/WhatIsTheOncotypeDXBreastCancerTest.aspx
http://www.tuorigen.cl/index.php/preguntas-frecuentes
http://www.cancer.gov/espanol/publicaciones/diccionario?cdrid=652256
http://www.lampadia.com/analisis/tecnologia/medicina-del-futuro-despliegue-de-un-nuevo-paradigma/
http://www.patia.com.mx/braca.html
https://breast-cancer.oncotypedx.com/es-MX/Professional-Invasive/WhatIsTheOncotypeDXBreastCancerTest.aspx
http://www.tuorigen.cl/index.php/preguntas-frecuentes
http://www.cancer.gov/espanol/publicaciones/diccionario?cdrid=652256
http://www.lampadia.com/analisis/tecnologia/medicina-del-futuro-despliegue-de-un-nuevo-paradigma/






Tu opinión es importante
Estás invitado a enviar cualquier comentario o aportación que quieras realizar, gracias.